
بما أنَّ الكثير من جراثيم البكتيريا (مثل بعض سلالات البكتيريا المسبّبة لمرض السيلان، أو تلك التي تسبّب اعتلالات في المعدة والأمعاء) أصبحت تقاوم المضادّات الحيوية بضراوة، أصبح لِزامًا على العلماء أن يجدوا أيّ حل لمثل هذه المشكلة، حتى ولو كان هذا الحل غير إعتيادي كاستخدام الفيروسات آكِلات البكتيريا (bacteriophages). ورغم أنَّ هذا المنحى غير جديد، فقد تمّ اكتشافه قبل قرنٍ من الزمن، إلا أنَّ استخدامه ظلّ موجودًا لدى الدول التي لم يكن في مقدورها الحصول على المضادات الحيوية سابقًا، واستمرت في استخدامها حتى اليوم، كما هو الحال في معهد إليافا الموجود في تيبليسي بجمهورية جورجيا وغيرها.
وقد توقّف استخدام المعالجة بالفاجات عندما تمّ تطوير المضادات الحيوية بدءًا من البينيسيلين في منتصف الأربعينيات من القرن الماضي، كون أنّ المضادات الحيوية حين اكتشافها وتطويرها بعد ذلك، تستطيع القضاء على الكثير من أنواع البكتيريا الممرضة بينما تكون الفاجات متخصصة في نوعٍ واحدٍ أو حتى سلالة واحدة. هذا بالإضافة إلى أنَّ إنتاج الفاجات وطرق تنظيم تشريعاتها وكونها تُعتبر كائناتٍ خاملة أو شبه حيَّة يتمّ إدخالها إلى الأبدان للعلاج. لكنَّ مخـزون المضادّات الحيوية الفعّـالة هذه الأيـام أصبح يتضاءل، ممّا حدا بالممارسين الصحيين أن يجرّبوا العودة إلى المعالجة بالفاجات كحلّ معقولٍ وسريعٍ لمشكلة مقاومة البكتيريا للمضادّات الحيوية، وهي مشكلة عالميَّة.
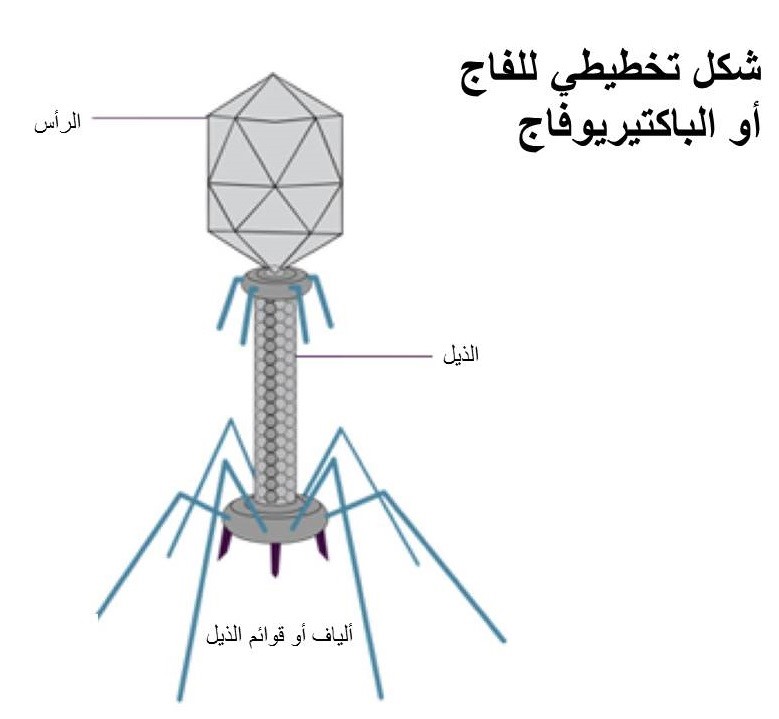
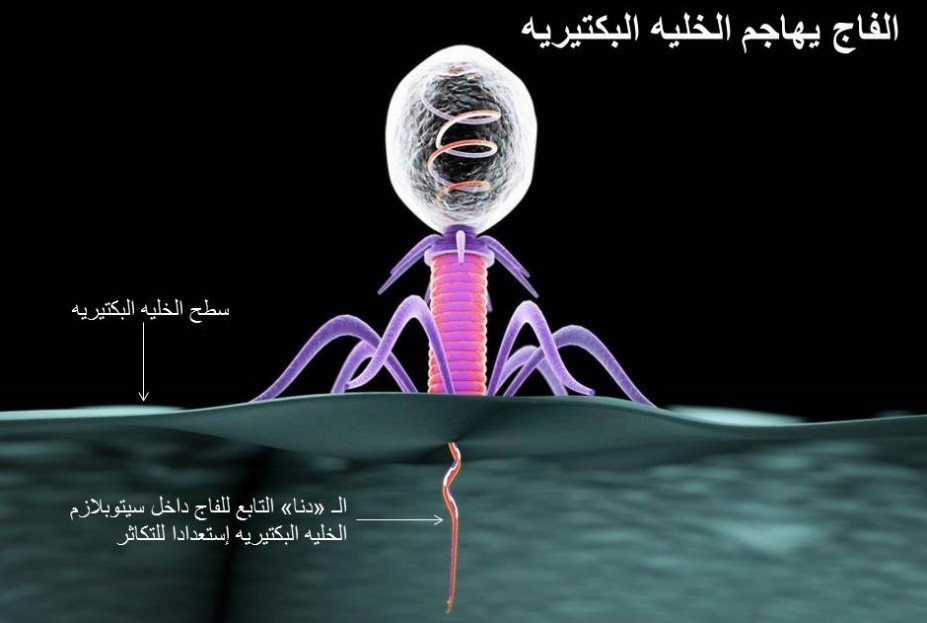
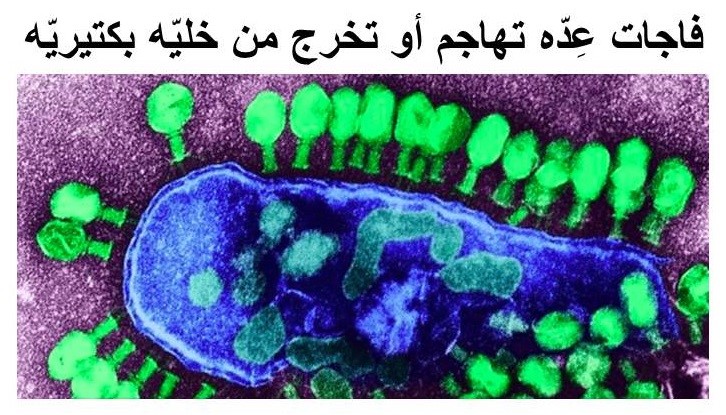
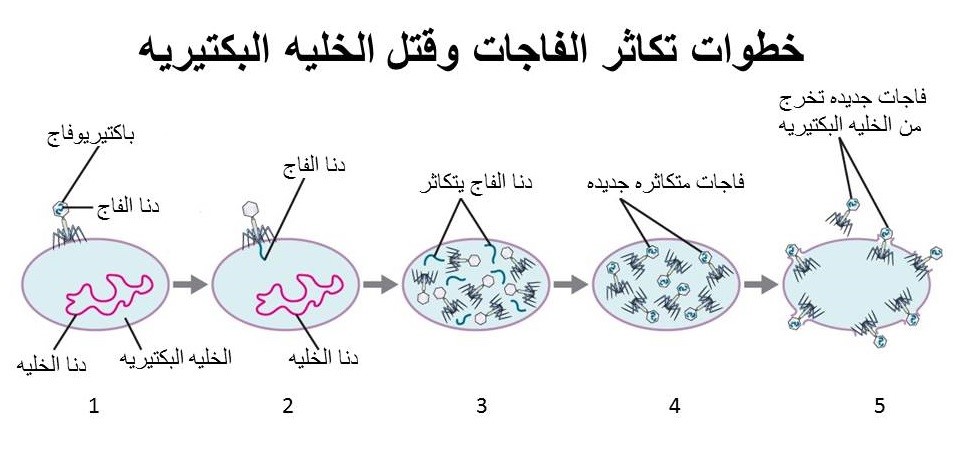
وبعكس المضادّات الحيوية والتي هي مواد كيماوية غالبًا ما تكون مُشيَّدة، فإنَّ الفاجات هي فيروسات، وبالتالي تستطيع التغيُّر والنُشوء، ممّا يعني أنَّ تغيُّر البكتيريا (لكي تكون مقاومة للمضادّات الحيوية مثلًا) يقابلها تغيُّر في الفيروسات التي تلتهمها، وكلاهما يتسابقان علي التطوُّر والتحوُّل منذ بلايين السنين. فالفاجات غير قادرة على النمو والتكاثر إلاّ إذا أدخلت في داخل الخلية البكتيرية مكوِّنها الوراثي (DNA) والذي يختطف تفاعلات الخلية اللازمة لنموّها ويسخِّرها لنفسه ولتكاثره كباقي الفيروسات، وتصبح الخلية كأنها مصنع لإنتاج هذه الفيروسات التي عندما تكثُر في العدد تنفجر الخليّة البكتيرية وتموت.
ويمكن للبكتيريا أن تصبح مقاوِمة لهذه الفيروسات بتغيير ماهية أسطحها الخارجيّة والمستقبِلات التي عليها، بحيث لا يمكن للفيروس أن يرتبط بها ومن ثمَّ يدخلها. إلاّ إنَّ الفيروسات أيضًا دائمة التحوُّل بحيث تستمر دائرة الحياة لها في الطبيعة. وكلما حاولت البكتيريا خداع الفيروس بتغيير شكلها يقوم الفيروس أيضًا بتغيير شكله لكي تستمر حياته بدخوله داخل البكتيريا الملائمة له، وهذا شيءٌ لا يمكن للمضادّات الحيوية أن تفعله. وبالإضافة لذلك، هناك استراتيجيّات أخرى لتفادي المقاومة مثل استخدام خليطٍ أو مزيجٍ من الفاجات المتخصصة في نوعٍ ما أو سلالة ما، حيث يقوم كل واحد من هذه الفاجات بمهاجمة الخلية البكتيرية عن طريق مستقبِل مختلف (كما هي الحال في معالجة فيروس نقص المناعة المكتسَب بإعطاء خليطٍ من الأدوية التي يهاجم كل واحد منها الفيروس بطريقةٍ مختلفة). ورغم أنّ هذه
الاستراتيجية تساهم بشكل فعّال في منع حدوث المقاومة البكتيرية من الأساس إلّا أن هناك مخاوف من احتمالية انتقال الجينات بين السلالات البكتيرية المختلفة عن طريق هذه الفيروسات البكتــيرية بما في ذلك جينات المقاومة، ولكن هذه الاستراتيجية تعطي طيفًا واسعًا من النشاط المضاد للبكتيريا.
ومن مزايا المعالجة بالفاجات هو أنَّ حساب الجرعة الفعّالة لها ليس بالأمر المهم كما هي الحال مع المضادّات الحيوية والتي تعتمد في فعّاليتها أساسًا على حساب الجرعة اللازمة للمعالجة والتي إن زادت عن الحاجة فيمكن أن تتسبّب في أعراض جانبيّة غير مرغوب فيها، وإن قلّت فلن تموت البكتيريا وتصبح مقاومة للمضاد الحيوي، فالفيروسات الملتهمة للبكتيريا تستطيع ضبط الجرعة آلياً بنفسها. ففي وجود البكتيريا تدخل الفيروسات وفي غيابها تتوقف هذه الفيروسات وتخرج من الجسم بدون إحداث مضاعفاتٍ تُذكَر.
ويحقّ للمرء إذًا أن يتساءل لماذا لا تكون المعالجة بالفاجات متوفّرة في أي مستشفى أو صيدليّة؟ والسبب في ذلك ببساطة هي أنّ المعالجة بالفاجات ليست لحد الآن مُوافَق و مُصادَق على إستخدامها من قِبل كثيرٍ من المؤسسات الرقابيّة في العالم رغم ثبوت فوائدها في بعض الدول مثل جورجيا وروسيا وبولندا وبلجيكا. وتنتظر هذه المؤسسات الرقابيّة نتائج التجارب السريرية العلمية، والاتّفاق على أسلوب ترخيصها للاستخدام حيث أنّها تُعتبر مواد حيّة تُستخدم للإنسان. ومن الجدير بالذكر أنّ كمية الفاجات التي تُعطى للمريض ومقدار جرعتها صعبة التحديد، لكون هذه الفاجات تتكاثر كي تقتل البكتيريا، وليس هناك طريقة محددة لمعرفة كميّتها بعد تكاثرها، هذا إذا تمَّ التأكّد من أنها وصلت للمنطقة المراد علاجها ولم تتوزَّع على نطاقٍ واسع. لذلك، فإن استخدام الفاجات موضعيًا هو السائد حاليًا في العلاج بالفاجات، إلّا في حالاتٍ خاصة تستوجب ما يسمى بالحالات الخاصة للاستخدام الرحيم. وقد فسحت بعض المؤسسات الرقابية استخدامها في الحيوانات والنباتات، وأعطت هيئة الغذاء والدواء الأمريكية منتجًا من الفاجات ضـد بعض أنواع بكتيريا السالمونيـلا وَصْف: "يعتبر آمن عمومًا"، وتمَّ بعد الموافقة الخاصة والرحيمة من هيئة الغذاء والدواء الأمريكية بعض الاستثناءات للمعالجة بالفاجات كتلك التي أُعطيت لمريض ببكتيريا الأسينيتوباكتر العالية المقاومة في المركز الطبي لجامعة كاليفورنيا في سان دييغو، وشُفِيَ المريض بدون أي مضاعفاتٍ أو أعراضٍ جانبيّة. وتقوم هيئة الدواء الأوروبية بعمل تجارب سريرية على نطاقٍ واسع في هذه الأيّام حتى يُمكن استخدام الفاجات في المعالجة بشكلٍ روتيني.
وقد أثبتت الملاحظات والتجارب أنّ الفاجات تعدّ آمنة عند استخدام الإنسان لها وغير ضارّةٍ له. وهذه الفاجات منتشرة في الطبيعة بشكلٍ كبيرٍ جدا، فهي متوفرة في الينابيع والتربة والمجاري وخلاف ذلك. ويُقَدَّر أنَّ أعدادها في الطبيعة تفوق أعداد البكتيريا بعشرات المرّات. فالإنسان يتعرّض لها بصفةٍ يومية ودائمة، وهي متخصصة بشكلٍ محدد في البكتيريا. وهناك من يرى أنّ البشر يتعرّضون للفاجات البكتيرية بشكلٍ يومي بسبب انتشارها الكبير في الطبيعة. وبالتالي فليس هناك من داعٍ للقلق من عدم أمانها. ولكن في سياق التجارب السريرية لا بدّ من الأخذ في الاعتبار نقاء وتعقيم المستحضر الفاجي بالإضافة للمخاوف المحيطة باحتمال حدوث صدمةٍ تسممية كنتيجةٍ لانفجار البكتيريا، بعد تكاثر الفاجات في داخلها ثم قتلها.
ومن المتوقّع في المستقبل القريب أن يقلَّ اعتماد مقدمي الرعاية الصحية على المضادات الحيوية، وخاصة تلك ذات الطيف الواسع، وسيكون التركيز على معالجة العدوى بطريقةٍ محددة (precision medicine). وبوجود الطرق الحديثة في تحديد التسلسل الجزيئي للمادة الوراثية، وحفظ هذه التسلسلات عن طريق التقنية المعلوماتية سيكون من السهل إعطاء خليطٍ من الفاجات المحددة لبكتيريا محددة لعلاج أنواع العدوى والالتهابات البكتيرية المختلفة.
وتجدر الإشارة إلى أنّ تطوير مثل هذه المعالجات لابد أن يحدث في بلادنا وبسرعة، فقد أصبح هذا التطوير موجودًا في بعض الدول المجاورة، وسوف يسهم بشكلٍ فعّال مستقبلًا في الأمن الدوائي لأوطاننا، فعجلة حدوث مقاومة البكتيريا للمضادات الحيويه تتسارع، ولأسبابٍ كثيرة ومختلفة ليس هناك من أسلحةٍ جديد يتم تطويرها ضد هذه الجراثيم، وهناك دراسات سريرية على استخدام المعالجة بالفاجات يتم إجراؤها حاليًا في كثيرٍ من دول العالم المتقدم.
مراجع مفيدة
– Kortright KE, Chan BK, Koff JL, Turner PE (2019) Phage Therapy: A Renewed Approach to Combat Antibiotic-Resistant Bacteria. Cell Host Microbe. 25(2):219-232. doi: 10.1016/j.chom.2019.01.014.
– Gordillo Altamirano FL, Barr JJ (2019) Phage Therapy in the Postantibiotic Era. Clin Microbiol Rev. 32(2):e00066-18. doi: 10.1128/CMR.00066-18.
– Górski A, Międzybrodzki R, Łobocka M, et al. (2018) Phage Therapy: What Have We Learned? Viruses. 10(6):288. doi: 10.3390/v10060288.
تواصل مع الكتاب: profahdal@gmail.com
الآراء الواردة في هذا المقال هي آراء المؤلفين وليست، بالضرورة، آراء منظمة المجتمع العلمي العربي
يسعدنا أن تشاركونا أرائكم وتعليقاتكم حول هذهِ المقالة عبر التعليقات المباشرة بالأسفل أو عبر وسائل التواصل الإجتماعي الخاصة بالمنظمة





