للبحث الدقيق يمكنك استخدام البحث المتقدم أدناه
يعتمد البحث السريع على الكلمات الموجودة داخل عنوان المادة فقط، أما البحث المتقدم فيكون في كافة الحقول المذكورة أعلاه
نتائج البحث
ثورة التحرير الجيني
-
 منصة النقاش
منصة النقاش
كُن الأول ... لفتح نقاش حول موضوع هذا المقال
-
الوقت
10:50 ص
-
تاريخ النشر
13 مارس 2017
الكلمات المفتاحية :
تخيل أنك تعلم أن عائلتك تحمل مرضا وراثيا كالتخلف العقلي، أو فقر الدم المنجلي، أو السكري من النوع الأول، أو بعض أشكال سرطان الثدي والبروستاتا والقولون، وإذا نجحت في إزالة الجين المسؤول عن هذا المرض في طفلك المستقبلي، فيمكنك الحصول على طفل سليم خال من هذا المرض! ... فمن المؤكد أنك لن تبخل ببذل كل نفيس وغال من أجل الحصول على هذا الطفل السليم، وستبذل أقصى جهد لتحقيق هذا الهدف النبيل. ولكن بطبيعة الحال فالأمر ليس سهلاً، ففي حالة بعض الأمراض الوراثية لابد من التلاعب بآلاف الجينات، للحصول على جنين لطفل خال من هذا المرض. ولكن تطوير العديد من تقنيات التحرير الجيني في الآونة الأخيرة قد يستطيع تحقيق مثل هذا الهدف صعب المنال، ونجحت بالفعل بعض من هذه التقنيات في تنفيذ عمليات التنقيح الجينومي، والإصحاح الجيني، والقيام بتعديلات مستهدفة ومحددة للجينات، ولها إمكانيات كبيرة لا حدود لها في المجالات العلمية التطبيقية.
- كريسبر .. تحرير الجينات أصبح سهلا
- المصدر :Ella Maru Studio/SPL
طرق التحرير الجيني
ومن المعروف أن هناك ثلاث طرق أساسية تسمح للعلماء بالتلاعب بالجينات وتغيير الخلايا الحية مثلما يمكن لمستخدم الكومبيوتر أن يغير أي نص يكتبه على ملف وورد مثلا فيستخدم القطع، واللصق، والاستنساخ والحذف وإزالة الحذف، والتكرار وما إلى ذلك لتغير النص الأصلي وتنقيحه. وتستخدم طريقة نيوكلييز إصبع الزنك على وجه الخصوص لحذف خلايا الدم البيضاء، ويؤمّل أنها بهذا الشكل ستفتح الباب للقضاء على فيروسات مرض نقص المناعة المكتسبة، من خلال الدخول إلى جهاز المناعة. وكانت هذه التقنية أول أداة لتحرير الجينوم لكنها محدودة القدرة لاعتمادها على بروتينات صعبة التكيف مع الجينات المستهدفة الجديدة، وقد تخطأ أحيانا وتقطع في مكان غير صحيح. أما الطريقة الثانية فهي طريقة تعتمد على الإنزيمات الشبيهة بمنشط التناسخ المحلّلة للنيوكلوتايدات المستجيبة (TALENs) وهي انزيمات تستخدم في قطع الحمض النووي ومناطق التصاقه، ويمكن برمجتها للتلاعب بجينات محددة، وهي أسهل من حيث التطبيق كما أنها أقل كلفة، لكنها هي الأخرى تفتقد إلى عنصر الدقة في القطع واللصق، وكان تطبيقها الناجح الأول قد جرى على رضيعة تبلغ عاما من العمر وتعاني من اللوكيميا.
أما طريقة "كريسبر-كاس9" أو (الموضع الصبغوي ذو التكرارات المُنتظمة المُتجمعة قصيرة التناوب) فهي الطريقة الأكثر شيوعا في الوقت الحاضر، وتعتمد على استخدام بروتين "كاس9" الذي يهاجم الحمض النووي للفيروسات كما لو انه "مقص"، بالإضافة إلى جزيئين بسيطين من أجل العثور على موضع بعينه من الحمض النووي بهدف التدخل لإصلاحه. وهي في الأساس عبارة عن سكين جزيئية حادة للغاية أو مقصًا جينيًا دقيق جدًا، وتسمح هذه الأداة للعلماء باقتطاع وإضافة الجينات بدِقة تامة وبتكاليف زهيدة، ويستطيع الباحثون باستخدام "كريسبر" للتخلص من جينات واستبدال جينات سليمة محل جينات معطلة في الحمض النووي أو إضافة مقاطع جينية جديدة لهذا الحمض. وتتميز تقنية "كريسبر" التي أحدثت ثورة غير مسبوقة في مجال التحرير الجيني عن التقنيات المنافسة لها بأنها رخيصة نسبيا وسهلة الاستخدام في عمليات التلاعب الجيني المتعدد، وأن لها القدرة على تعديل التتابعات الوراثية المميزة لأي حمض نووي. وقد بدأت بعض الشركات باستخدام هذه التقنيات لأغراض علاجية في تجارب إكلينيكية عدة، وأثبتت "كريسبر" سهولة استخدامها وقلة تكلفتها مقارنةً بغيرها من التقنيات، وتوفير الخيارات المتعددة والمتعلقة بعملية استهداف الجينات.
- مثل المقص في هذه الصورة، الإنزيم كاس9 يقطع الحمض النووي. ويمكن أن يبرمج لإيجاد وربط مواقع معينة في الجينوم.
- المصدر:https://vector.childrenshospital.org/2014/09/genome-editing-a-crispr-way-to-correct-disease
- الإنزيم كريسبر (الأحمر والأخضر) يقيد إلى امتداد الحمض النووي مزدوج الجديلة (الأرجواني والأحمر) استعدادا لقص الجزء المعيب من الجينوم.
- المصدر: Jennifer Doudna/UC Berkeley.
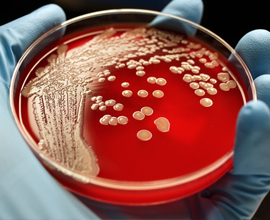
يشار إلى أن فكرة هذه التقنية ولدت في عام 2007 بعد أن اكتشفت شركة للألبان الرائبة وبشكل مفاجئ آلية دفاعية قامت باستخدامها بعض أنواع البكتيريا لمقاومة الفيروسات. ثم جاء إعلان الولادة في عام 2012، تبعتها خطوات أولية هامة في عام 2013 إلى أن تطورت التقنية بشكل كبير خلال العام الفائت. والآن تطورت أكثر إلى أن حالت إلى ما يشبه الأعجوبة الجزيئية، حيث أصبح العالم بأسره مهتماً بتقنية "كريسبر" والتي تعتبر الإنجاز العلمي الأهم للعام 2015م، ورُشحت مرتين بالفعل لنيل جائزة نوبل.
- تصدرت تقنية كريسبر غلاف مجلة ساينس كأهم اختراق علمي لعام 2015م.
- المصدر: Science: 12/18/2015, Vol 350 Issue 6267.
وتستطيع هذه التقنية التدخل في تغيير المجموع الجيني لجميع الكائنات الحية بدءاً من البكتيريا والنبات والحيوان وصولاً للإنسان وذلك بشكل فعال. وبررت دورية "ساينس" اختيارها المقص الجيني على رأس أبرز الإنجازات العلمية لعام 2015 بقولها إنه يمهد لإدخال تغييرات جينية على الحشرات تجعلها تفقد القدرة على تحمل الأمراض. ويأمل الباحثون بأن تمكننا هذه التقنية في يوم ما من استئصال أو إزالة الجينات الشريرة المسببة للأمراض، وبخاصة الوراثية منها، ويرى الباحثون أنها ليست إلا مسألة وقت فقط قبل أن تُستَخدَم هذه الأداة لهندسة ذريتنا والتخلص من العديد من الأمراض الوراثية الخطيرة في هذه العملية.
تعتبر كريسبر الإنجاز العلمي الأهم لعام 2015م، ورشحت مرتين بالفعل لنيل جائزة نوبل: ولاقت تقنية "كريسبر" نجاحًا لا يُصدق في البحوث العلمية، مؤدية إلى نمو هائل في الأوراق البحثية التي تتناول موضوعهُا، وتُمكّن هذه التقنية العُلماء من تعديل الجينوم بكفاءة ومرونة ودقة لم يسبق لها مثيل، فاتحةً الأفاق لأبعاد جديدة لتعديل الجينوم لأغراض مُختلفة ابْتِداءً بعلم الأعصاب والهندسة الوراثية وصولاً إلى بيولوجيا النبات. وبشرت "كريسبر" بعصر جديد من الهندسة الوراثية، عصر قد يسمح لنا بحماية محاصيلنا من الجفاف والعدوى، ومحو الأمراض الوراثية في البشر وغيرها من الأنواع، وحتى عكس الشيخوخة، ولقد استولت تقنية "كريسبر" على عالمنا، فقد تَغلغلت في كُل مجالات الصناعة تقريباً، مُبرهنة على أن محدودية استخداماتها هي في مُخيلتنا فقط.
الصين تفوز بقصب السبق: ومن الأمثلة الشهيرة لتطبيقات هذه التقنية هي إجراء أول تعديل جيني لأحماض نووية خاصة بأجنة بشرية غير قابلة للحياة في إحدى عيادات الخصوبة في الصين، والذي تصدر عناوين الأخبار، ونتج عن هذا الإعلان تعجيل إقامة قمة دولية لمناقشة موضوع التعديل الجيني البشري.
وقد ناقشت القمة تصحيح الجينات الخاصة بالأمراض أو عمل تحسينات عليها في السائل المنوي البشري أو البويضات أو الأجنة في صورتها الأولية. وكان العلماء في الصين قد قاموا بعملية تعديل وراثي في أجنة من أجل تعديل أحماض نووية فيها خلل تؤدي إلى ولادة طفل مع أمراض في الدم أسبابها وراثية. في حين أن السلطات البريطانية المختصة سمحت للعلماء بالبدء في أبحاث التعديل الوراثي للأجنة، فيما أعلن معهد فرانسيس كريك في لندن عن شروعه في بحث يهدف إلى "فهم أعمق للحظة الأولى لحياة الجنين لدى البشر" وذلك فور سماح السلطات البريطانية بذلك. وفى حقيقة الأمر تتمتع الصين بشهرة على قدرتها على التقدم السريع فيما يتعلق بالتقنيات الحيوية البازغة، وبشكل خاص تقنية التحرير الجيني كريسبر. وتحتل الصين مكان الصدارة عندما يتعلق الأمر بالتحرير الجيني لأن الصين تُولِي أولوية عالية للبحوث الطبية الحيوية. وأعلن نجاح مجموعة من الباحثين الصينيين في التعديل الوراثي للأجنة البشرية لتكون محصنة ضد فيروس نقص المناعة البشرية (الإيدز)، مظهرين بذلك الإمكانيات الهائلة للتحرير الجيني، عن طريق إكساب مناعة ضد الفيروس بطريقة مماثلة لعمل اللقاح ولكن على المستوى الجيني أو الوراثي، وإذا ما وصلت هذه التقنية إلى المراحل الإكلينيكية، فإنه من الممكن استخدامها للقضاء على جميع أنواع الأمراض الوراثية. وفى الوقت الحالي تتوالى الاكتشافات والابتكارات التي تعتمد على هذه التكنولوجيا يوما بعد يوم.
وأصبح العلماء الصينين الرواد على مستوى العالم في استخدام البشر في تجاربهم لتكنولوجيا التحرير الجيني، وخاصة مرضي سرطان الرئة؛ حيث حصل الفريق الذي يترأسه لو يو طبيب الأورام في مستشفى غرب الصين في جامعة سيتشوان فى تشنجدو على التصديق (الإقرار الأخلاقي) من مجلس مراجعة المستشفى ببدء اختبار هذه الخلايا في أشخاص مصابين بسرطان الرئة في السادس من يوليو 2016م.
ويقوم الفريق حاليًا باختبار الخلايا ذات الجينات المحرَّرة على الأشخاص الذين يعانون من سرطان الرئة. وتضم التجربة الصينية مرضى سرطان الرئة النقيلي ذي الخلايا غير الصغيرة، الذين لم يجدي معهم العلاج الكيماوي ولا الإشعاعي ولا أي علاج اخر. وقام فريق لو باستخراج الخلايا المناعية المعروفة باسم الخلايا التائية، أو الليمفاويات التائية وهي نوع من خلايا الدم البيضاء، من دم المشاركين. وباستخدام تكنولوجيا "كريسبر-كاس9" تمكنوا من دمج دليل جزيئي قادر على تحديد التسلسل الجيني النوعي على كروموسوم مع إنزيم يمكنه قَصّ هذا الكروموسوم في تلك البقعة؛ لتعطيل جين يقوم بترميز بروتين يُسمى PD-1، يعمل عادةً ككابِح لقدرة الخلايا على إطلاق استجابة مناعية تتصدي لهجمات و تهديدات الخلايا الأخرى. ومن ثم، تتم مضاعفة الخلايا محررة الجين في المختبر، وإعادة طرحها في مجرى دم المريض، حيث يأمل الفريق في أن تقوم الخلايا المحررة جينيًا باستهداف السرطان وتثبيط البروتين بدقة أكبر، وزيادة مقاومة الخلايا السرطانية.
أطفال حسب الطلب
ربما سيكون بوسعنا قريباً تعديل الحمض النووي (DNA) للبشر، لمعالجة أمراض مثل السرطان؛ ولكن هل سيقود ذلك إلى ظهور مواليد مُعدلين جِينياً للحيلولة دون إصابتهم بأمراض بعينها أو لضمان اتسامهم بصفات أو ملامح معينة؟ إذا ما حدث ذلك، فمن المتوقع أن تضطلع الصين بدور رائد في هذا الشأن؛ كما يقول جي. أوين شيفر العالم المتخصص في مجال قيم وأخلاقيات علم الأحياء. ومن المؤكد أن هذا الاحتمال يخضع الآن لمناقشات محتدمة، وتتلخص الحجج الرئيسية ضد إجراء التعديل الوراثي على أجنة بشرية في أن هذه الممارسة ستكون غير آمنة وغير عادلة، وأن التعديل سرعان ما يتجاوز الجهود الرامية إلى الحد من انتشار الأمراض الموروثة. ولكن في نهاية المطاف، من غير المرجح أن تكون أي من هذه الأسباب مقنعة بالقدر الكافي لمنع استخدام هذه التقنية على نطاق واسع.
وقد زادت حدة هذا النقاش بعد ابتكار تقنية تعديل الصفات الوراثية "كريسبر- كاس 9"، والتي زادت من الإمكانيات المخيفة للعبث بالحمض النووي للإنسان، بهدف تحسين صفاتٍ مثل الذكاء واللياقة البدنية، والقدرة على ممارسة الرياضة بشكل جيد، بل وحتى الحس الأخلاقي، وتطوره. قاد التمويل الذي وفرته حكومة بكين الصين في عام 2015 لتصبح أول دولة تجري تعديلات على جينات أجنة بشرية باستخدام تقنية "كريسبر-كاس 9". كما كان للصين الصدارة على طريق الاستعانة بهذه التقنية، لإجراء تعديلات جينية – لا تمس "الخط الإنتاشي" – لخلايا أنسجة بشرية، بهدف الاستفادة منها في علاج مرضى السرطان.
وتثير السهولة التي يمكن بها تنفيذ هذا التحرير الجيني الخوف من أن يكون الإنسان التالي. وقد يعترض البعض بحكم أنّ هذا النوع من التدخل هو اعتداء على وظائف الإله، وهو اعتراض يشبه الاعتراضات التي ظهرت أيام تطبيق تقنيات حيوية أخرى مثل عمليات التخصيب المختبري المعروفة بـ "أطفال الأنابيب"، وأبحاث الخلايا الجذعية. ويقول منتقدو هذه البحوث الجديدة أن العلماء لا ينبغي لهم "اللعب" بالأجنة البشرية بهذا الشكل، بحجة أن الأجنة من الرئيسيات الأخرى من شأنها أن تؤدي نفس الغرض. هناك أيضاً القلق من أن هذه التعديلات قد تنتقل إلى الجيل التالي، الأمر الذي يمكن أن يؤدي إلى عواقب غير متوقعة. ويخشى العلماء من أن تتسبب الهندسة الوراثية في دفع الأزواج إلى الهندسة الوراثية للأجنة في رحم الأم الأمر الذي يدفع إلى التحكم بصورة وكيفية ولادة المولود وخاصة بما يتعلق بجنسه، وقضايا أخرى مثل هندسة شكل الطفل.
علاوة على ذلك، يأمل العلماء ألا تطغى الأسئلة الأخلاقية بشأن بعض استعمالات "كريسبر" على فاعلية هذه التكنولوجيا وتؤخر حصولها على موافقة السلطات المعنية. ويقول منتقدو هذه البحوث الجديدة أن هناك قلق من أن هذه التعديلات الوراثية قد تنتقل إلى الجيل التالي، الأمر الذي يمكن أن يؤدي إلى عواقب غير متوقعة. ويخشى العلماء من أن تمكن هذه التقنيات الأزواج من هندسة الأجنة وراثيًا، فضلا عن التحكم في اختيار جنس المولود بالصورة والكيفية التي يرغبها الأبناء، والعديد من القضايا الشائكة الأخرى مثل هندسة شكل الطفل، واختيار خصائصه على أسس جينية.
ويرى الباحثون أنها ليست إلا مسألة وقت فقط قبل أن تستخدم هذه التقنيات لهندسة ذريتنا والتخلص من العديد من الأمراض الوراثية الخطيرة. فهل نحن على شفا "عالم جديد شجاع"؟ .. مثل ذلك الذي تناوله الكاتب ألدوس هُكسلي في روايته التي تحمل نفس الاسم، وهو عالم يقطنه بشر مُحسنين وراثياً؟ ربما يكون هذا صحيحاً. وهناك فكرة جديدة مثيرة للاهتمام في هذا الصدد بأنه من المنطقي الاعتقاد بأن أي تحولٍ مدوٍ في مجال "التحسين الوراثي" سينشأ من الصين على الأرجح، ولن يبزغ من دول غربية، مثل الولايات المتحدة والمملكة المتحدة، وهي دول شكلت مهداً للعديد من التقنيات الحديثة.
بريد الكاتب الالكتروني: tkapiel@sci.cu.edu.eg

هذا والموقع يساعد المؤلف على نشر إنتاجه بلا مقابل من منفعة معنوية أو مادية، شريطة أن يكون العمل متوفراً للنسخ أو النقل أو الاقتباس للجمهور بشكل مجاني. ثم إن التكاليف التي يتكبدها الموقع والعاملون عليه تأتي من مساعدات ومعونات يقبلها الموقع ما لم تكن مرتبطة بأي شرط مقابل تلك المعونات.
ترخيص عام
الموقع قائم على مبدأ الترخيص العام للجمهور في حرية النسخ والنقل والاقتباس من جميع المحتويات والنشرات والكتب والمقالات، دون مقابل وبشكل مجاني أبدي، شريطة أن يكون العمل المستفيد من النسخ أو النقل أو الاقتباس متاحا بترخيص مجاني وبذات شروط هذا الموقع، وأن تتم الاشارة إلى منشورنا وفق الأصول العلمية، ذكرا للكاتب والعنوان والموقع والتاريخ.





0 التعليقات